¿Su mascarilla o respirador filtra virus vivos?
No todas las mascarillas quirúrgicas, mascarillas médicas y respiradores (en adelante, «mascarillas») que cumplen los estándares normativos europeos o estadounidenses deben someterse a pruebas con virus vivos, solamente se hacen pruebas con partículas sólidas (por ejemplo: partículas saladas) o bacterias (cuyo tamaño es aproximadamente 100 veces mayor que el de los virus).
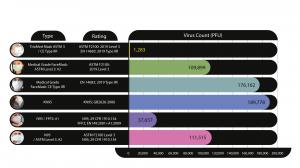
Las únicas normas reguladas que se utilizan actualmente en América y Europa y que incluyen pruebas de la eficacia de filtración de microbios son respectivamente la ASTM 2100 norteamericana y la norma europea EN14683 de eficacia de filtración bacteriana (BFE, por sus siglas en inglés). Aunque no es un requisito gubernamental, se acepta la sustitución de las bacterias por un virus vivo para probar la eficacia de filtración de virus (VFE, por sus siglas en inglés). Estos protocolos de ensayo estandarizados requieren una concentración de 10^5 virus por litro de aire durante un tiempo de prueba de solo 2 minutos, por lo que solo se calcula la eficacia de filtración de las «mascarillas» durante 2 minutos de uso. Se encargó a GAP EnviroMicrobial Services Ltd. que comprobara la eficacia de filtración de virus siguiendo los mismos protocolos pero con un tiempo de prueba de 30 minutos, a la velocidad del aire de 85 lpm que recomienda NIOSH1, y en diversas mascarillas (quirúrgicas, médicas/quirúrgicas ASTM nivel 3, CE tipo IIR, KN 95, N95 y FFP2). Las pruebas mencionadas anteriormente se realizan solamente en los materiales filtrantes de las mascarillas según indican los requisitos del protocolo.
A modo de referencia, si un sujeto infectado tose una sola vez puede liberar un promedio de 4 914 600 partículas virales aerosolizadas2. Averigüe si su mascarilla o respirador filtra virus vivos en las tablas incluidas.
Para obtener más información sobre las mascarillas TrioMed Active, visite www.triomed.com o envíe un correo electrónico a triomed@triomed.com
Acerca de i3 Biomedical Inc.: i3 Biomedical es una empresa canadiense de dispositivos médicos, centrada en el desarrollo y la fabricación de productos antimicrobianos innovadores con la tecnología TrioMed Active.
Acerca de GAP EnviroMicrobial Services Ltd.: GAP EnviroMicrobial Services Ltd. (GAP), creada en 1996, cumple la norma ISO/IEC 17025:2005 con la acreditación de la Asociación Canadiense para la Acreditación de Laboratorios (CALA, por sus siglas en inglés), que cuenta con el reconocimiento de casi 60 organismos de acreditación en 40 países de todo el mundo.
1 Instituto Nacional para la Seguridad y Salud Ocupacional
2 Lee, J., Yoo, D., Ryu, S., Ham, S., Lee, K., Yeo, M., Min, K. y Yoon, C. (2019). Quantity, SizeDistribution, and Characteristics of Cough-generated Aerosol Produced by Patients with anUpper Respiratory Tract Infection (Cantidad, distribución del tamaño y características del aerosol generado por tos producido por pacientes con infección del tracto respiratorio superior). Aerosol Air Qual. Res. 19: 840-853. https://doi.org/10.4209/aaqr.2018.01.0031
Pierre Jean Messier
i3 Biomedical Inc.
triomed@triomed.com
Visit us on social media:
Facebook
Twitter
Legal Disclaimer:
EIN Presswire provides this news content "as is" without warranty of any kind. We do not accept any responsibility or liability for the accuracy, content, images, videos, licenses, completeness, legality, or reliability of the information contained in this article. If you have any complaints or copyright issues related to this article, kindly contact the author above.